Biología sintética: la primera célula viva artificial
Miguel Ángel Cevallos
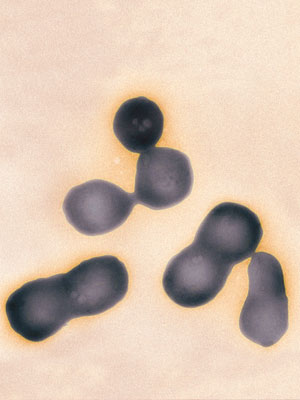
Imagen: T. Deerinck y M. Ellisman / UCSD
El pasado 20 de mayo se dio a conocer una noticia que ha causado demostraciones tanto de júbilo como de completa consternación: la creación de una célula bacteriana controlada por un genoma sintético. ¿Cuáles son los antecedentes de esta investigación y sus posibles consecuencias?
Puedo afirmar —y no dudo en meter mi mano en el fuego por ello— que estamos viviendo los inicios de lo que se conocerá como la era de la biología molecular, la cual tendrá un impacto quizá mayor o por lo menos equivalente al descubrimiento y desarrollo de la energía atómica que tuvo lugar en la primera mitad del siglo xx. Durante las últimas décadas hemos acumulado una enorme e invaluable cantidad de datos sobre la naturaleza de la información genética. Nuestro conocimiento es especialmente sólido en las bacterias, que son los organismos celulares más simples y más abundantes en la Tierra. Tenemos una idea bastante clara acerca de cómo funcionan los genes bacterianos, en qué forma interactúan unos con otros, con cuáles patrones —dependiendo de las condiciones ambientales— se encienden y se apagan, y cómo adquieren nueva información genética estos microorganismos. A este entramado de conocimientos tenemos que sumarle el inmenso arsenal de nociones que hemos obtenido mediante el análisis de los más de 1 000 genomas bacterianos que se han secuenciado hasta la fecha. Este arsenal es especialmente relevante, ya que nos permite analizar, a semejanza de lo que hace un ingeniero cuando revisa los planos de un edificio complejo, el plano de vida de un organismo. Un grupo creciente de investigadores afirma que ya poseemos un cuerpo de conocimientos de tal magnitud que podemos realizar nuestros propios diseños basados o inspirados en lo que ocurre en la naturaleza, y en consecuencia aseguran que estamos ante las puertas de lo que hoy en día, de manera tal vez un tanto presuntuosa, pero desde luego no infundadamente visionaria, empieza a ser denominado biología sintética.
Diseño genético
El término biología sintética no es nuevo en el lenguaje científico: surgió en los años 80 para referirse a la tecnología requerida para la producción de las primeras bacterias modificadas genéticamente que poseían uno o pocos genes ajenos a su patrimonio genético original; sin embargo, hoy por hoy el término tiene una connotación mucho más amplia, ya que se refiere a la ciencia y a las técnicas utilizadas para diseñar y construir bloques de genes que confieran a los organismos características y funciones nuevas, que no existen en la naturaleza. Y con ello me refiero no sólo a la modificación de microbios para que tengan, digamos, la capacidad de degradar compuestos sintéticos o producir biocombustibles, sino también, en última instancia, a la creación de nuevos organismos vivos, diseñados en el escritorio, y luego generados a partir de ingredientes químicos obtenidos en el laboratorio.
Dicho lo anterior, parece muy probable que surjan juicios encontrados: así, algunos opinarán que estamos frente al nuevo Frankenstein; para otros será el fin del vitalismo, posición filosófica que sostiene que la vida no se crea, se transmite, y, por lo tanto, asegura que el principio vital de algún modo es independiente de la estructura de la célula.
En general, los biólogos están de acuerdo en que todos los seres vivos deben cumplir con tres requisitos para que pueda considerarse que realmente están vivos: primero, ser capaces de automantenerse, es decir, tener un metabolismo; segundo, poder reproducirse; y tercero, poseer la capacidad de evolucionar. Esto es muy fácil de decir, pero establecer exactamente qué compuestos, qué genes y qué proteínas se requieren para cumplir esos tres requisitos, es algo muy diferente.
Uno de los puntos de vista más controversiales que sostienen los científicos involucrados en la biología sintética es que aseguran tener un acercamiento experimental para resolver el dilema más importante de la biología: entender los principios fundamentales del fenómeno al que llamamos vida. Su propuesta es que si queremos saber qué es la vida, la tenemos que sintetizar en el laboratorio, bajo condiciones experimentales estrictas. El primer paso firme ya se ha dado.
 Células en división de M. mycoides artificial. Imagen: T. Deerinck y M. Ellisman / UCSD
Células en división de M. mycoides artificial. Imagen: T. Deerinck y M. Ellisman / UCSD
Organismos artificiales
El día 20 de mayo de este año recibimos una noticia extraordinaria, que seguramente cambiará el curso de la biología como ciencia y tendrá, en un futuro no muy lejano, repercusiones enormes en nuestra vida cotidiana. Ese día, Daniel Gibson, Craig Venter y otros 22 científicos del Instituto J. Craig Venter de Estados Unidos publicaron, en la influyente revista Science, un artículo cuyo titulo lo resume todo: “Creación de una célula bacteriana controlada por un genoma sintetizado químicamente”. Y lo resume todo porque, en otras palabras, la lectura del artículo revela varias primicias trascendentales: que, por primera ocasión, el material genético de un organismo (genoma) se diseña por métodos bioinformáticos (computacionales); que ese material genético se sintetiza químicamente y se trasplanta a una célula huésped, para dar origen a un organismo nuevo cuyas funciones dependen exclusivamente de las instrucciones que se le introdujeron. Los científicos más entusiastas opinan que se trata de la primera vez que se genera vida en el laboratorio; los más conservadores incluso están de acuerdo en que éste es un paso inicial, pero firme, para crear una célula viva completamente artificial.
 Mycoplasma mycoides artificial. Imagen: J. Craig Venter Institute.
Mycoplasma mycoides artificial. Imagen: J. Craig Venter Institute.
Los inicios
El artículo aparecido en Science es el resultado de muchísimos años de arduo trabajo, durante el cual se tuvieron que sortear innumerables obstáculos. Muy probablemente, la génesis de este proyecto ocurrió cuando Craig Venter (ver recuadro) se propuso, hace 15 años, determinar la secuencia del material genético de la bacteria patógena Haemophilus influenzae. Con las técnicas actuales, esta meta se pudo haber alcanzado, literalmente, en unos cuantos días; sin embargo, hace década y media obtener la secuencia completa del adn de una bacteria era un proyecto visionario, complicado y de alto riesgo, puesto que en ese entonces apenas surgían los primeros secuenciadores automáticos de adn, y se carecía de herramientas computacionales para enfrentar ágilmente el problema. Muchos consideran que en realidad el nacimiento de las ciencias genómicas tuvo lugar mucho antes, el 28 de julio de 1995, fecha en que se publicó el artículo que daba cuenta de este proyecto.
Haber elegido Haemophilus influenzae como objeto de estudio fue una decisión muy inteligente, puesto que se trata una bacteria que puede crecer en condiciones de laboratorio, cuyo genoma se sabía pequeño y, por lo tanto, más fácil de secuenciar. Pocos meses después, el Dr. Venter y su equipo determinaron la secuencia del genoma de otra bacteria, Mycoplasma genitalium, que también crece en el laboratorio, pero en condiciones mucho más estrictas que las que requiere Haemophilus, pese a que tiene un genoma mucho más pequeño que el que posee esta última. La idea subyacente en estos proyectos era determinar cuál es el número mínimo de genes requerido para que una célula pueda ser considerada como viva. En 1996, y luego de sesudos análisis comparativos entre los genomas de Mycoplasma y Haemophilus realizados con herramientas bioinformáticas, los doctores Koonin y Mushegian, de los Institutos Nacionales de Salud (NIH) de Estados Unidos, estimaron que ese número mínimo es de 256 genes. Diez años después, Craig Venter y sus colaboradores decidieron cotejar experimentalmente esta aproximación. Con ese fin, se empeñaron en destruir uno a uno los genes de Mycoplasma genitalium para determinar cuáles genes son esenciales para la vida y cuáles no. Así establecieron que 100 genes de esta bacteria son completamente prescindibles, y llegaron a la conclusión de que solamente se necesitan 425 genes para generar un organismo con vida independiente, más de los predichos por Koonin y Mushegian, pero aún así un número de genes ridículamente bajo para un fenómeno que se consideraba intrínsecamente complejo. Con estos números en mente, Venter percibió que era concebible sintetizar químicamente un genoma pequeño y “darle vida”, transplantándolo a una célula huésped. Desde ese entonces, esto es, desde 2006, Venter y su equipo se dedicaron a establecer los protocolos científicos para hacer que este sueño se concretara, lo cual ocurrió cuatro años después. Desde un inicio, a este grupo de científicos le quedó perfectamente claro que había que resolver dos problemas clave que, además, podían solucionarse independientemente uno del otro. El primero era establecer cómo se podría trasplantar un genoma a una célula huésped y lograr que éste sustituyera al original y así “tomara” el control de las funciones celulares. El segundo se centraba en cómo sintetizar químicamente un genoma.
¿Quién es John Craig Venter?
Lo menos que se puede decir del científico estadounidense Craig Venter, nacido en 1946, es que es un personaje controvertido; algunos lo califican de pedante e incluso de mercachifle, otros aseguran que es el científico más influyente del siglo y que su visión está cambiando la forma en la que se hace ciencia. Su perspectiva de la relación entre la ciencia y la industria también es radical y por ello se ha ganado más de un enemigo. Venter, bioquímico de formación, recibió un doctorado en fisiología y farmacología de la Universidad de California, en 1975. Trabajó, inicialmente, en la Universidad Estatal de Nueva York y luego en los Institutos de Salud de los Estados Unidos, donde planteó la importancia de identificar los genes que desempeñan un papel fundamental en la fisiología del cerebro. Con este fin, Venter determinó la secuencia parcial de un número enorme de los mensajes genéticos (ARN mensajeros) que se sintetizan en ese órgano. Venter, en una acción muy publicitada, intentó patentar estos genes, pero afortunadamente los tribunales no se lo permitieron. Pocos años después cofundó la compañía Celera Genomics, y ahí se convirtió en el primer científico que obtuvo la secuencia genómica completa de un organismo vivo: Haemophilus influenzae. Lo consiguió a través de una estrategia novedosa llamada shotgun sequencing, que combinaba el poderío de los secuenciadores automáticos con los de la bioinformática. Con esta experiencia en mano, Venter retó al consorcio internacional que estaba a cargo de secuenciar el genoma humano afirmando que él cumpliría esta meta en mucho menos tiempo y a menor costo. Y así fue: él secuenció el genoma humano, el suyo propio, en tiempo récord. Esta compañía también secuenció los genomas de la mosca de la fruta, del ratón, de la rata y del perro (el poodle de Venter). A Venter lo obligaron a abandonar Celera Genomics cuando se concluyó que no se podía fácilmente sacar provecho económico de este tipo de información. En otra contribución, Venter se propuso explorar la diversidad microbiana de los océanos a través de la secuencia masiva de los genomas de los microorganismos que ahí habitan. Esta estrategia novedosa para describir los componentes bacterianos de un ecosistema se conoce ahora como metagenómica (ver ¿Cómo ves?, No. 73) y ahora se utiliza ampliamente para explorar, por ejemplo, las bacterias que habitan nuestra piel y nuestro intestino, en distintas condiciones de salud y de dieta. Desde mi punto de vista, el diseño y la construcción de la primera célula sintética, que esbozo en este artículo, será un parteaguas en la historia de la ciencia. Además del Instituto que lleva su nombre y que cobijó el proyecto de la primera célula artificial, Venter ha fundado otras compañías como Synthetic Genomics, cuya meta es generar microorganismos modificados genéticamente para la producción de energías alternativas como el etanol y el hidrógeno. Venter está más activo que nunca y estoy seguro que nos sorprenderá nuevamente con sus propuestas y sus descubrimientos.
 Colonias de la bacteria Mycoplasma mycoides artificial. Imagen: J. Craig Venter Institute.
Colonias de la bacteria Mycoplasma mycoides artificial. Imagen: J. Craig Venter Institute.
Los primeros éxitos
Contra todos los pronósticos, estas metas se resolvieron rápidamente: en 2007, Venter y colaboradores publicaron en Science un artículo intitulado “Trasplantes de genomas en bacterias: cambiando una especie en otra”, en el cual daban cuenta de cómo resolvieron el primer problema. Meses después, en la misma revista salió publicado otro artículo de dichos autores, cuyo título era “Síntesis química completa, ensamblaje y clonación del genoma de Mycoplasma genitalium”, con el que anunciaban que habían resuelto el segundo problema. Es decir, en 2008 ya tenían establecida una metodología para crear, por vez primera en la historia, un célula sintética viva.
Durante los dos años siguientes, los investigadores del Instituto J. Craig Venter pulieron sus estrategias experimentales y replantearon sus metas: la primera de ellas fue establecer que el genoma ideal para trabajar no era el de Mycoplasma genitalium, sino el de su primo hermano Mycoplasma mycoides, un organismo de genoma más grande, pero mucho más fácil de manejar en el laboratorio; la segunda meta fue utilizar como célula huésped a otro primo hermano: Mycoplasma capricolum, parecido en muchos sentidos al anterior, pero con características distintivas tanto genéticas como fisiológicas que permiten diferenciar perfectamente las dos especies de Mycoplasma.
 Ilustración: Raúl Cruz Figueroa
Ilustración: Raúl Cruz Figueroa
Célula artificial
Para asegurar el éxito de estos experimentos, Venter y sus compañeros decidieron que en un inicio era más prudente imitar a la naturaleza, así es que se impusieron la tarea de diseñar un genoma muy parecido al de Mycoplasma mycoides, pero incluyendo en él ciertas diferencias genéticas —a las cuales llamaron, como si fueran papel moneda, marcas de agua— con el único propósito de hacer que el genoma artificial fuera fácilmente distinguible del nativo, y descartar cualquier tipo de contaminación.
El equipo de los doctores Gibson y Venter construyó el genoma artificial empleando un método similar al que se utiliza para diseñar y fabricar un rompecabezas, y luego para armarlo. Ante todo, para crear un rompecabezas es indispensable tener bien clara la imagen que se quiere plasmar; una vez delineada esa imagen, es preciso elaborar las piezas del rompecabezas pensando en que sean del mismo tamaño, y desde luego, en que no se repitan. Cuando ya se procede a armar el rompecabezas, el procedimiento usual consiste en unir las piezas por grupitos, y al final, ensamblar todos estos grupitos para reconstruir la imagen diseñada. Del mismo modo, el equipo de Gibson y Venter sintetizó químicamente 1 078 fragmentos de adn, cada uno de ellos con una longitud de poco más de 1 000 pares de bases (pb), que abarcaban la totalidad del genoma diseñado. Luego ensamblaron los fragmentos de 10 en 10, para acabar con una colección de 109 fragmentos más grandes a los que llamaremos casetes de cerca de 10 000 pb cada uno. Es muy importante subrayar que este primer ensamblaje se hizo, aunque parezca una locura, dentro de la levadura de la cerveza (Saccharomyces cerevisiae). Esto se debe a que se han desarrollado manipulaciones genéticas que permiten “pegar” pedacitos de adn en un orden preestablecido, de una manera ágil y barata, dentro de este microorganismo. Este procedimiento puede hacerse perfectamente en el tubo de ensayo, según estos mismos autores han demostrado, pero en esa forma resulta más lento y más costoso.
La tercera etapa del proyecto consistió en purificar los 109 casetes y “pegarlos”, nuevamente en grupitos de 10, en un orden establecido, para así lograr 11 segmentos ensamblados de alrededor de 100 000 pb cada uno, utilizando asimismo la levadura como vehículo para hacer esta manipulación genética. En la siguiente etapa se procedió de manera similar: se purificaron los 11 segmentos de 100 000 pb y se pegaron, con la misma estrategia, en el orden requerido y de esta manera llegar finalmente a una sola molécula de aproximadamente 1.1 millones de pb, que corresponde precisamente al genoma completo artificial previamente diseñado. Posteriormente, el genoma artificial se extrajo de la levadura.
Gibson y Venter tenían bien claro que si querían trasplantar exitosamente su genoma artificial ante todo debían evadir el sistema de defensa de la célula huésped, pues las bacterias poseen enzimas, conocidas como enzimas de restricción, que destruyen cualquier adn que provenga de fuera. Este mecanismo, obviamente no surgió para hacerles la vida difícil a los investigadores, sino para destruir el material genético de los virus que las infectan. Las bacterias han desarrollado, al mismo tiempo, enzimas que modifican su propio adn (metilasas), a fin de evitar que las enzimas de defensa confundan lo propio con lo ajeno y lo destruyan. Por ello, estos investigadores purificaron las enzimas de protección de adn de Mycoplasma capricolum, y las usaron para proteger su genoma artificial.
Para poder lograr el trasplante, se incubó el adn protegido del genoma sintético con las células de Mycoplasma capricolum, en presencia de un sustancia (polietilenglicol) que promueve la entrada del adn a las células. Por un mecanismo que todavía no se entiende a cabalidad, las células que reciben el genoma sintético eliminan el propio.
Otro reto importante al que tuvieron que enfrentarse estos investigadores fue el de buscar una manera eficiente de reconocer a las pocas células en las cuales ocurrió el trasplante, distinguiéndolas de aquellas células huésped que permanecieron sin cambio. Con este fin, mañosamente introdujeron en el genoma sintético, además de las marcas de agua, que ya mencioné, dos propiedades que están ausentes en el genoma de las células huésped: un gen que confiere resistencia al antibiótico Tetraciclina y otro gen que provoca que las células se vuelvan azules en presencia de un reactivo químico especial. Comprobaron así que las células en las que ocurrió el trasplante se volvieron azules en presencia de este reactivo y crecieron en medio de cultivo con Tetraciclina. Para que nadie tuviera dudas acerca de su trabajo, los científicos purificaron el genoma de las células trasplantadas, lo secuenciaron y certificaron que todas las marcas de agua que introdujeron en el diseño original estaban realmente ahí presentes.
Las células con el genoma sintético fabricaron poco a poco nuevos componentes celulares, siguiendo las instrucciones presentes en el nuevo genoma, hasta sustituir por completo todos los componentes de la célula original, como posteriormente demostró el equipo de Gibson y Venter. Hasta ese momento, se obtuvo, por fin, una célula cuya estructura y fisiología depende exclusivamente del genoma artificial.
Para poder lograr el trasplante, se incubó el adn protegido del genoma sintético con las células de Mycoplasma capricolum, en presencia de un sustancia (polietilenglicol) que promueve la entrada del adn a las células. Por un mecanismo que todavía no se entiende a cabalidad, las células que reciben el genoma sintético eliminan el propio.
Otro reto importante al que tuvieron que enfrentarse estos investigadores fue el de buscar una manera eficiente de reconocer a las pocas células en las cuales ocurrió el trasplante, distinguiéndolas de aquellas células huésped que permanecieron sin cambio. Con este fin, mañosamente introdujeron en el genoma sintético, además de las marcas de agua, que ya mencioné, dos propiedades que están ausentes en el genoma de las células huésped: un gen que confiere resistencia al antibiótico Tetraciclina y otro gen que provoca que las células se vuelvan azules en presencia de un reactivo químico especial. Comprobaron así que las células en las que ocurrió el trasplante se volvieron azules en presencia de este reactivo y crecieron en medio de cultivo con Tetraciclina. Para que nadie tuviera dudas acerca de su trabajo, los científicos purificaron el genoma de las células trasplantadas, lo secuenciaron y certificaron que todas las marcas de agua que introdujeron en el diseño original estaban realmente ahí presentes.
Las células con el genoma sintético fabricaron poco a poco nuevos componentes celulares, siguiendo las instrucciones presentes en el nuevo genoma, hasta sustituir por completo todos los componentes de la célula original, como posteriormente demostró el equipo de Gibson y Venter. Hasta ese momento, se obtuvo, por fin, una célula cuya estructura y fisiología depende exclusivamente del genoma artificial.
 Mycoplasma capricolum.
Mycoplasma capricolum.
Más información
- www.gen-es.org/12_publicaciones/docs/pub_75_d.pdf
- www.biologia-sintetica.org/biosistemas
Perspectivas
El anuncio de la construcción de la primera célula artificial ha causado demostraciones tanto de júbilo como de completa consternación. Muchos investigadores están convencidos que ésta es una nueva avenida para construir, de manera fácil y económicamente rentable, bacterias que fabriquen, por ejemplo, medicamentos novedosos o biocombustibles; también existen otros para los que estas innovadoras tecnologías hacen factible producir organismos que sirvan de biosensores para vigilar el medio ambiente o mejor aún, para estudiar las bases de la vida misma. Pero también hay muchos científicos que temen que esta tecnología recién nacida constituya el camino para crear inauditas y más potentes armas biológicas. Otros temen que no podamos evaluar todavía las consecuencias ecológicas del “escape” al medio ambiente de alguno de los futuros organismos artificiales. Ante la noticia, el Vaticano expresó que la nueva tecnología puede ser un desarrollo positivo si se usa correctamente, no sin dejar clara su firme creencia en que sólo Dios es capaz de crear la vida. Bajo este abanico de opiniones y de confusas perspectivas, Estados Unidos y los países que conforman la Unión Europea —y espero que México no se quede atrás— están organizando foros de bioética que sopesen la situación, analicen las consecuencias de esta nueva ciencia y establezcan códigos de ética, evidentemente muy necesarios.
Para concluir, me gustaría recalcar que las tecnologías no son buenas ni malas, todo depende de cómo se usen. Por ejemplo, la pólvora puede usarse en los festivos fuegos artificiales o en una bomba. La morfina puede usarse como un analgésico maravilloso o como una droga terriblemente adictiva. La energía atómica se puede usar para borrar de un solo golpe a una ciudad entera, o proveerla de toda la energía eléctrica que necesita. Así es que informar y reflexionar cuidadosamente sobre las nuevas tecnologías es esencial para promover su uso adecuado.
Miguel Ángel Cevallos, frecuente colaborador de ¿Cómo ves?, es doctor en investigación biomédica básica y especialista en genética molecular bacteriana. Trabaja en el Centro de Ciencias Genómicas de la unam y está dispuesto a recibir estudiantes interesados en realizar un posgrado














