Fármacos y vacunas contra el nuevo coronavirus
Miguel Ángel Cevallos

Ilustración: balabolka/Shutterstock
Las estrategias que se están usando para encontrar un tratamiento y una vacuna contra la COVID-19 lo antes posible se basan en el conocimiento científico del virus que la causa y cómo infecta a los seres humanos.
Al momento de escribir este artículo, en el mundo se han enfermado de COVID-19 más de 20 millones de personas y han muerto cerca de 740 000. A pesar de lo grave de la situación estoy convencido de que las soluciones a mediano y largo plazo están en manos de la ciencia, siempre y cuando los políticos reconozcan su valía y apoyen su implementación.
La ciencia en acción
La manera en que la ciencia ha enfrentado la pandemia es un ejemplo de su eficacia y versatilidad. A los pocos días de que se reconoció que había un brote de neumonía atípica en China causada por un virus, este se pudo aislar y se desentrañó la secuencia de su material genético, información que se depositó inmediatamente en bases de datos internacionales para que cualquier persona pudiera tener acceso a ella. Con estos datos se logró establecer con certeza que el responsable de la enfermedad es un nuevo coronavirus y en solo unas semanas se determinó cuáles son sus componentes y el papel que tienen en su ciclo de vida. De algunos de ellos, los más relevantes, se pudo establecer su estructura tridimensional por técnicas de cristalografía y de técnicas computacionales de modelaje de proteínas. Esto es esencial para el desarrollo de fármacos y vacunas contra el nuevo coronavirus. También, en tiempo récord, no solo se logró establecer cómo se propaga el virus, sino también el mecanismo por el cual se replica dentro de nuestras células y el curso evolutivo que está tomando.
Los parientes del nuevo coronavirus
El material genético del nuevo coronavirus (SARS-CoV-2) es una cadena enorme de ARN de casi 30 000 nucleótidos, uno de los genomas más grandes de virus de ARN que se conocen. La secuencia del genoma es en sí misma invaluable, ya que nos permite en primer lugar reconocer cuáles son los parientes más cercanos del virus. En segundo, echar por tierra todas esas ideas conspirativas que afirmaban que este virus se había escapado de un laboratorio y, por último, determinar de dónde surgió y cuáles son sus componentes estructurales.
Cuando se contrastó la secuencia del genoma de este nuevo virus contra las secuencias de otros virus depositadas en bases de datos, se determinó que el causante de la COVID-19 (la enfermedad que produce el SARS-CoV-2) era un nuevo beta-coronavirus, emparentado con otros dos de la misma familia que causaron epidemias serias en el pasado reciente: el virus causante del SARS (Síndrome Agudo Respiratorio Severo) y el virus del MERS (Síndrome Respiratorio del Medio Oriente).
También se descubrió que se parece muchísimo, en más del 96 %, al genoma de otros beta-coronavirus que se han aislado de murciélagos, su reservorio natural, y a algunos beta-coronavirus aislados de pangolines; mamíferos que se comercian ilegalmente en China. Estas observaciones permiten establecer que el origen del SARS-CoV-2 ocurrió primero cuando un coronavirus que se encontraba originalmente en los murciélagos adquirió la capacidad de infectar a otro tipo de animales, posiblemente pangolines, y después algunas mutaciones adicionales le permitieron infectar a los humanos.
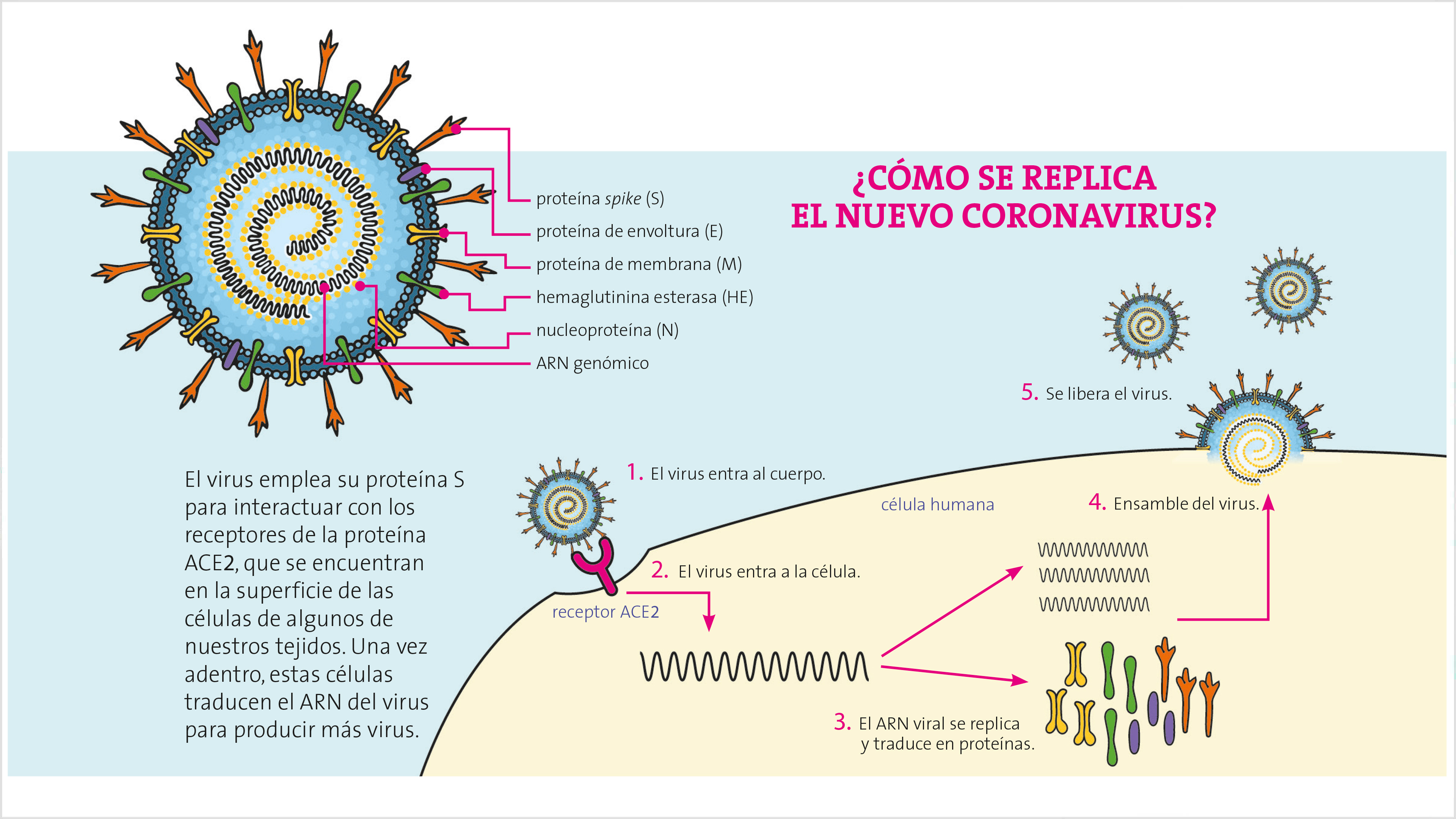
Retrato del SARS-CoV-2
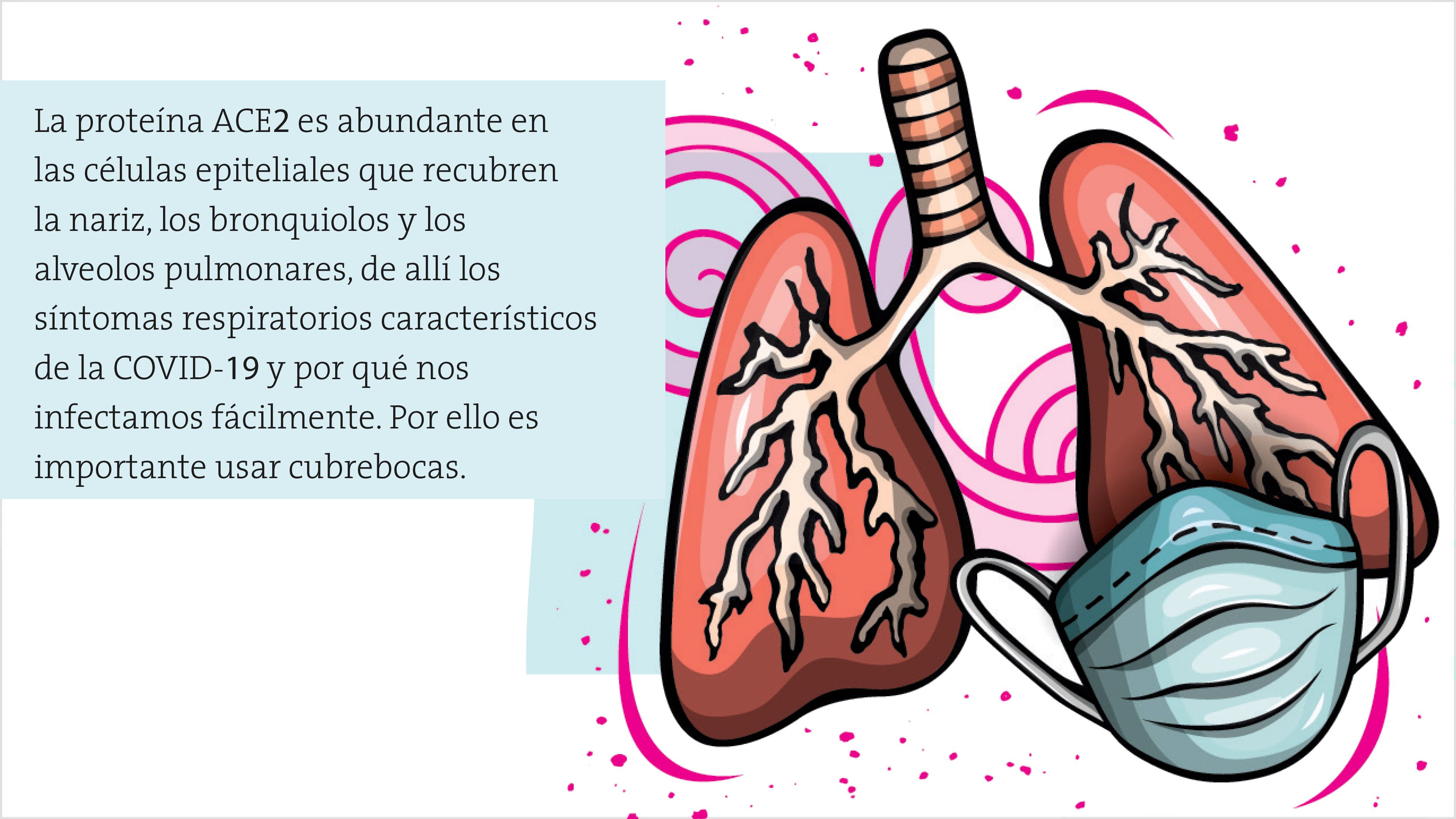
El análisis del genoma indica que el genoma del nuevo coronavirus tiene las instrucciones para producir 20 proteínas, pero solo cuatro de ellas están presentes en el virus maduro (virión) y por ello se les llama proteínas estructurales. Las otras 16 son importantes en la replicación del genoma viral y en la formación de nuevas partículas virales. La primera de las proteínas estructurales, la S (por spike, espícula), es la que le da al virus su peculiar forma de corona cuando se observa al microscopio electrónico y a través de ella el virus reconoce qué células puede infectar e iniciar el proceso de invasión. Este reconocimiento inicial ocurre cuando la proteína S interacciona con la proteína ACE2 (del inglés, Angiotensin-converting enzyme 2), receptor que se encuentra en la superficie de las células de algunos de nuestros tejidos. La ACE2 es particularmente abundante en las células epiteliales que recubren la nariz, los bronquiolos y los alveolos pulmonares. La localización de la ACE2 explica los síntomas respiratorios que caracterizan a la COVID-19 y por qué nos podemos infectar fácilmente si estamos en contacto con las gotas y los aerosoles (gotas más pequeñas) que produce una persona enferma al estornudar, toser, hablar o cantar. Esto hace evidente que el uso del cubrebocas es muy importante para protegernos y proteger a los demás. Quiero recalcar que la ACE2 es una proteína cuya función original no es capturar al coronavirus, sino que se relaciona con la regulación de la presión arterial.
Para que la proteína S del virus interaccione con la ACE2 tiene que ser procesada por una enzima que se encuentra en la superficie de muchas de nuestras células y que la corta en dos segmentos: solo así se puede iniciar el proceso de infección. La proteína M es la más abundante del virus y está inserta en la membrana que lo recubre. Se piensa que la proteína M contribuye a que el virus tenga una forma esférica. Por su parte, la proteína E (envoltura) se encuentra en bajas cantidades, pero es importantísima para que el virus se ensamble correctamente y posteriormente sea liberado de las células infectadas. Por último, la proteína N (nucleocápside) tiene una sección que se encuentra embebida en la membrana del virus y otra que se “asoma” a su parte interna. La proteína N hace contacto con el genoma viral y lo organiza para que se disponga de manera ordenada dentro de la partícula viral. Al encontrarse en la superficie del virus, las cuatro proteínas estructurales son los elementos que primero detecta nuestro sistema inmune y le indican que debe producir anticuerpos contra ellas.

¿Por qué necesitamos un buen diagnóstico?
Una herramienta esencial para el manejo adecuado de esta y otras pandemias es un diagnóstico ágil y preciso para identificar a las personas infectadas, ofrecerles los cuidados adecuados y aislarlas el tiempo necesario para evitar que contagien a otras personas. Esto es especialmente relevante en la fase 1 de una contingencia epidemiológica, es decir cuando aparecen los primeros brotes epidémicos en un país determinado debido a personas que se contagiaron en el extranjero y regresan enfermos (casos importados). Trazar adecuadamente estas primeras cadenas de contagio es muy útil para contener una epidemia. Esta estrategia fue especialmente útil para controlar eficientemente al SARS y al MERS, enfermedades que fueron mucho más letales (porcentaje de las personas infectadas que murieron) de lo que es ahora la COVID-19. Las personas infectadas enfermaron rápidamente y se quedaban varadas en sus casas. Además, solo aquellas que mostraban síntomas de la enfermedad eran contagiosas. El problema más serio que tenemos ahora para controlar la pandemia es que hay muchas personas infectadas que no presentan síntomas, pero son transmisoras del virus. Todo esto complica enormemente rastrear todas las cadenas de contagios. Y para dificultar aún más las cosas, los síntomas que caracterizan a la COVID-19, como la fiebre, el dolor de cabeza, la tos seca, el cansancio, etc. también son propias de otras enfermedades virales. Así es que un diagnóstico preciso es esencial no solo para combatir la pandemia, sino para canalizar los recursos humanos y económicos de una manera adecuada.

Pruebas para detectar el virus
Los sistemas de diagnóstico con los que contamos para detectar al SARS-CoV-2 se basan todos en la amplificación de un pedacito de su material genético, exclusivo de este virus, que no está presente en otros coronavirus que circulan en la población humana (alfa-coronavirus) y son responsables de un porcentaje considerable de los resfriados que sufrimos año con año. Para el diagnóstico solo se necesita una muestra de secreción nasofaríngea del paciente sospechoso de estar infectado, tomada con un hisopo, de la cual se aísla material genético del virus si es que está presente. En general los resultados se obtienen en unas horas, pero si los laboratorios que hacen la prueba están saturados, los resultados tardarán algunos días.
También podemos identificar quiénes estuvieron enfermos, aunque no hayan presentado síntomas, gracias a que las personas curadas, convalecientes o que tengan al menos siete días de infectadas tienen en la sangre altos niveles de anticuerpos contra el virus. Las pruebas rápidas se basan en detectar estos anticuerpos con un dispositivo semejante a las pruebas de embarazo. Este proceso es tan eficiente que los resultados se pueden obtener en pocos minutos.
Las personas con altos niveles de anticuerpos contra el virus ya no se pueden volver a enfermar, al menos mientras esos niveles sigan altos. En el caso del SARS y del MERS se pudieron detectar anticuerpos hasta un año después de la infección. Todavía no sabemos qué ocurre con la COVID-19, pero podría ser menos tiempo.
Las personas que resultaron positivas en la prueba rápida y han dejado de tener síntomas por algunos días ya no son contagiosas; no es necesario que sigan en cuarentena. Si las pruebas rápidas se aplican masivamente (lo que no sucede en México) las autoridades de salud pueden identificar gente infectada que no tiene síntomas y cortar así las cadenas de transmisión. Además, permiten determinar con mayor certidumbre quiénes han tenido contacto con el virus y evaluar si ya estamos saliendo de la pandemia o no. Vigilar el curso de la epidemia contabilizando solo los casos sospechosos seguramente implica subestimarla, sobre todo en aquellos lugares donde hay saturación de los hospitales.
Las pruebas rápidas también podrían tener un papel relevante para determinar en un centro de trabajo, por ejemplo, si los empleados pueden ingresar y retomar con seguridad sus tareas.
Terapias y medicamentos
Uno de los problemas de la COVID-19 es lo variado de sus síntomas y la intensidad de los mismos. Hay personas que no muestran síntomas o estos son leves, mientras que otras mueren en las unidades de cuidados intensivos. Existen factores que ayudan a que la COVID-19 se torne grave, como la edad, el sexo (los hombres fallecen significativamente más que las mujeres) y las llamadas comorbilidades, es decir, se enferman más seriamente quienes ya sufren otros padecimientos como la diabetes, la obesidad, la hipertensión, el cáncer o los problemas de corazón. Hay otro elemento a tomar en cuenta: muchos de los pacientes que se ponen graves lo hacen no porque el virus les esté ganado la batalla, sino porque su sistema inmune reacciona tan violentamente que ataca a sus propios tejidos. A este fenómeno se le conoce como tormenta de citocinas, ya que estas son las moléculas que producimos precisamente para modular la respuesta inmune; si se producen de más nos pueden llevar a la tumba.
Antes de empezar a hablar de medicamentos, hay que tener claro que para desarrollar una nueva molécula con valor terapéutico se necesitan aproximadamente 10 años de investigación y desarrollo; es el tiempo que toma asegurarse de que realmente sirva, que no tenga efectos secundarios nocivos y que haya sido aprobada por las instancias de salud correspondientes, como la Comisión Federal para la Protección contra Riesgos Sanitarios de nuestro país. El costo de desarrollar moléculas con valor médico se ha calculado en unos 800 millones de dólares. Así que empezar de cero no es la mejor estrategia. Lo que se está haciendo es probar fármacos ya conocidos y probados para otras enfermedades o infecciones virales, que potencialmente pudieran tener un efecto contra el nuevo coronavirus. Si se encuentra alguna molécula que tenga, aunque sea una acción parcial, se puede modificar químicamente buscando potenciar esa acción.
Las estrategias actuales para combatir médicamente la COVID-19 pueden clasificarse a grandes rasgos en dos grupos. El primero es encontrar fármacos que eviten que el virus nos infecte o bloqueen su ciclo de vida. Con muchos de ellos se busca impedir que el virus se pegue e invada nuestras células, ya sea bloqueando el receptor ACE2 o interrumpiendo la función de la proteína estructural S del virus. Una de las maneras que se están experimentando es engañar al virus con proteína ACE2 soluble o incorporada en nanopartículas. Si hay un exceso de ACE2, el virus encontrará estos señuelos moleculares y así se evitará que contacte a los ACE2 de nuestras células. Los experimentos hechos en ratones y en algunos pacientes son prometedores.
También se están probando fármacos contra el virus del sida que inhiben la enzima que corta en dos segmentos a la proteína S, evitando que se active y el virus entre a nuestras células. Otro enfoque es probar fármacos que inhiben las enzimas que participan en la replicación del virus y que han funcionado con éxito en infecciones provocadas por otros virus de ARN. En la misma línea, también existen medicamentos que se conocen como análogos de nucleótidos, diseñados para que el sistema de replicación de un virus se equivoque y genere genomas anómalos y no funcionales. Sin embargo, la terapia que promete tener éxito a corto plazo es usar el suero sanguíneo de pacientes convalecientes, con altos niveles de anticuerpos contra el virus. Este suero, suministrado por vía intravenosa, permitiría que el organismo del enfermo usara estos anticuerpos para combatir el virus sin esperar la respuesta inmune propia.
El segundo grupo de estrategias utiliza fármacos que evitan la inflamación exacerbada y la tormenta de citocinas. Uno de los medicamentos que se están probando es el interferón-beta, una citocina útil en el tratamiento de la esclerosis múltiple y que también sirve para combatir los efectos secundarios de algunas infecciones. Las pruebas piloto muestran que podría ayudar a enfrentar la COVID-19. También existen anticuerpos producidos en el laboratorio, como el Tocilizumab, que bloquean la acción de una de las citocinas que es fundamental para que ocurra la tormenta de citocinas. Recientemente la prensa le ha dado mucha atención a la dexametasona, un fármaco que se utiliza comúnmente en el tratamiento de la artritis y de ciertas alergias; hay evidencias de que ayuda sensiblemente a los enfermos de la COVID-19 que están graves, no así a quienes muestran síntomas menores. En cuanto a la hidroxicloroquina, un medicamente barato y eficaz contra la malaria y del que se pensaba podría ser útil contra el nuevo coronavirus, se ha encontrado que no funciona y además provoca una mortalidad mayor en pacientes de la COVID-19.

Vacunas
Muchos gobiernos y algunas compañías farmacéuticas están desarrollando diversos tipos de vacunas contra el SARS-CoV-2. Un recuento de las estrategias que se están siguiendo para lograrlo apareció en la revista Nature el 28 de abril de este año. Lo que hace una vacuna es engañar al cuerpo para que monte una respuesta de defensa eficiente sin necesidad de enfermarse. Es fácil decirlo, pero complicado hacerlo, ya que hay que determinar experimentalmente que la vacuna sea capaz de inducir anticuerpos que neutralicen al virus y que no provoque efectos secundarios de consideración. Todas las vacunas y medicamentos nuevos tienen que evaluarse clínicamente en tres fases. La primera es con voluntarios sanos para evaluar si la vacuna realmente despierta la respuesta inmune. La segunda fase se hace con más personas y la tercera usualmente incluye a miles de individuos; el objetivo es determinar la eficacia y seguridad de la vacuna. Ya hay ocho vacunas que están en la fase III de evaluación. La más avanzada es la de la compañía biotecnológica Moderna, que la está probando en 30 000 personas. Le siguen muy de cerca las vacunas de la compañía alemana Pfizer-BioNTech, la compañía china Sinopharm y la Universidad de Oxford en colaboración con la compañía AstraZeneca. El 11 de agosto Rusia anunció que ya aprobó una vacuna, pero esta solo se ha probado en 76 personas y no ha completado la fase III. Por desgracia no basta tener una buena vacuna, también hay que fabricarla y distribuirla y esto es una empresa titánica. En el mejor de los casos la vacuna estará lista y accesible en varios meses, así que la mejor manera de librarse de la COVID-19 es evitar infectarse aplicando las medidas sanitarias recomendadas. ¡Cuídense!
Comisión Universitaria para la Atención de la Emergencia Coronavirus: https://covid19comisionunam.unamglobal.com/?s=vacunas- “Intensificar la producción de vacunas”, Organización Mundial de la Salud, en: www.who.int/bulletin/volumes/98/5/20-020520/es/
- “Vacuna contra el COVID-19”, Organización Panamericana de la Salud, en: www.paho.org/es/tag/vacuna-contra-covid-19
Miguel Ángel Cevallos,frecuente colaborador de ¿Cómo ves?, es doctor en investigación biomédica básica y especialista en genética molecular bacteriana. Trabaja en el Centro de Ciencias Genómicas de la UNAM.














