Caras vemos, microbiotas no sabemos
Mariana Mastache-Maldonado
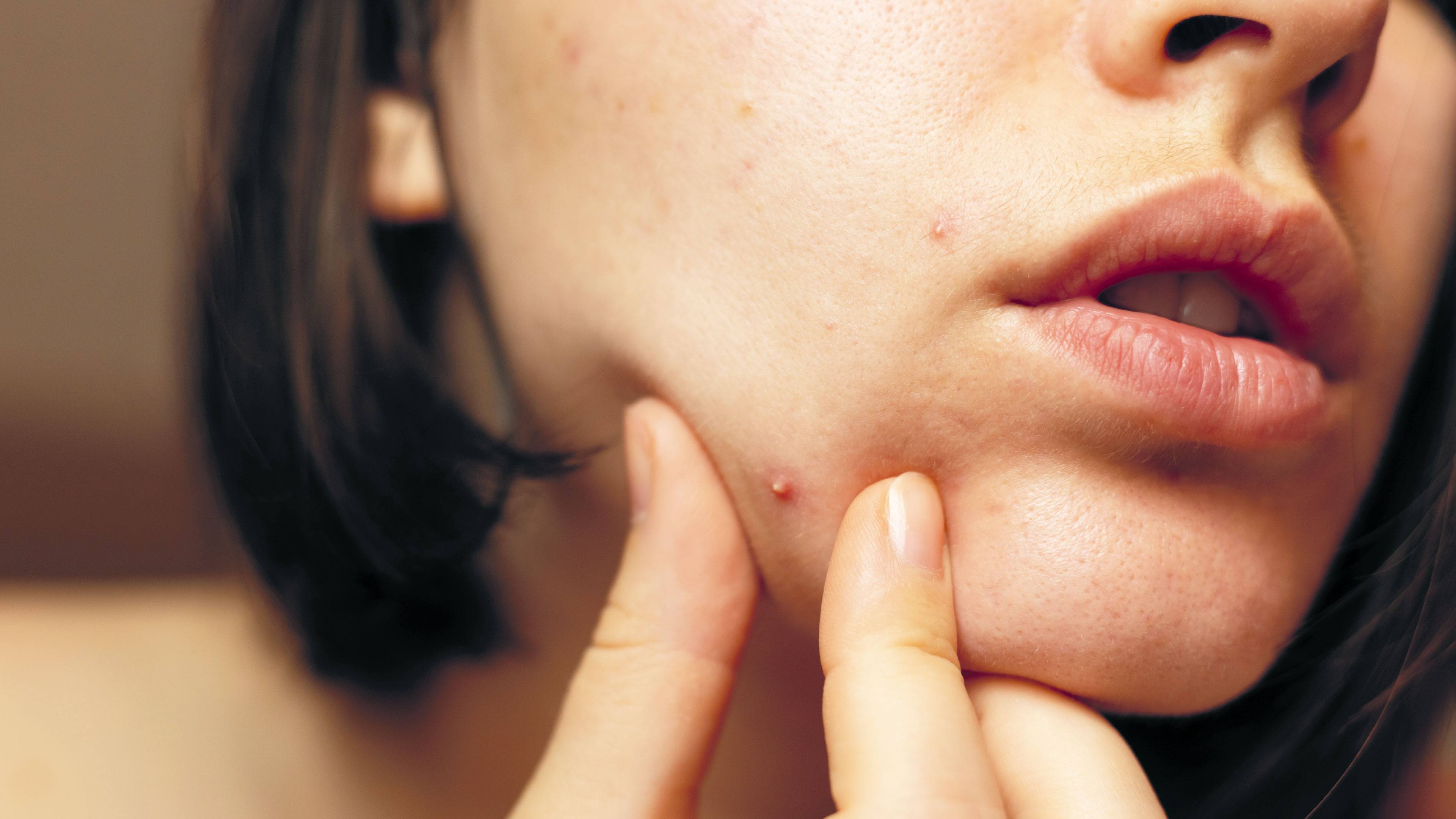
Foto: Shutterstock
Cada vez que salimos de casa llevamos con nosotros lo esencial: celular, dinero, llaves… y muchas vidas diminutas. Sí. Microbios.
Desde que nacemos adquirimos un traje de bacterias, virus y hongos que usaremos toda la vida. Y mientras más investigamos, más entendemos este ecosistema de cientos o miles de especies de seres diminutos. Hoy sabemos que en un cuerpo humano hay más genes de ellos que propios y que cumplen tantas funciones que hay quienes los llaman “el órgano oculto”. En pocas palabras, somos simbiontes. Nunca estamos solos.
Estos microbios que nos colonizan desde que somos bebés forman diversos nichos en diferentes partes del cuerpo, que conocemos como microbiotas. Cuando cumplimos tres años nuestra microbiota alcanza la diversidad que nos acompañará por el resto de la vida, pero también evolucionará con nosotros. Es decir, desde muy pequeños ya estamos colonizados por la cantidad de especies que tendremos para siempre, pero muchas cosas, entre ellas nuestro estilo de vida, determinará el equilibrio entre estas especies: a veces habrá más de unas, a veces más de otras.
Una de las microbiotas más conocidas es lo que antes llamábamos flora intestinal: los microbios del intestino, que cuando están en equilibrio contribuyen a mantener la salud. Pero no es la única. También tenemos microbiotas en el estómago, los ojos (¡sí, increíble!), los oídos, el tracto nasofaríngeo, los pulmones y la boca.
Y en la superficie de la piel: cada centímetro está cubierto por su propia microbiota. Cuando se altera el equilibrio de los microorganismos que la colonizan (un fenómeno conocido como disbiosis) pueden surgir enfermedades de la piel, claro, pero también otras que afectan varios sistemas del cuerpo.
Bienvenidos welcome
Cada parte de la piel tiene su “microambiente” o ecosistema. Esto se debe a las diferencias en la cantidad de luz ultravioleta que recibe, al pH, la temperatura, la humedad, el sebo (la grasa que produce la piel) y la forma del área; todo esto promueve o inhibe el crecimiento de diversas especies de microorganismos. Las zonas de la piel se agrupan en tres categorías: sebáceas (cara, pecho y espalda), húmedas (curva del codo, parte posterior de la rodilla e ingle) y secas (antebrazo y palmas).
Un estudio sobre el microbioma de la piel sana de los Institutos Nacionales de Salud de Estados Unidos encontró que en las áreas sebáceas predominan las bacterias del género Cutibacterium (el microbioma incluye los genes y el ambiente de los microorganismos). En las zonas húmedas, como los codos y los pies, son más comunes las bacterias Staphylococcus y Corynebacterium. Por su parte, los hongos del género Malassezia dominan en el torso y los brazos, mientras que los pies tienen una mayor diversidad de hongos como Aspergillus y Cryptococcus. Algunos de estos microorganismos son comensales, es decir que se benefician sin afectar a su huésped. Otros son simbiontes: tanto ellos como nosotros nos beneficiamos de esa interacción.
Una herramienta de la metagenómica es la secuenciación shotgun, una técnica que permite determinar la secuencia del adn de un organismo. Con este método el genoma se fragmenta en pequeñas porciones que se secuencian individualmente, y luego un programa informático detecta las superposiciones, las ensambla en el orden correcto e intenta construir el genoma completo lo mejor posible. Con ella se han estudiado varios ambientes extremos: zonas volcánicas, de alta temperatura, acidez o alcalinidad, bajo oxígeno y alta concentración de metales pesados… Pero también, en una escala más pequeña, entornos como el microbioma intestinal humano. Y se quiere extender lo mismo a las demás partes del cuerpo.
Cultivar microbios uno por uno en el laboratorio es un desafío, porque viven en entornos en los que el pH, el oxígeno y los nutrientes cambian continuamente, y replicar esas condiciones es extremadamente difícil. Por eso, para este estudio los investigadores usaron un enfoque metagenómico, que analiza el genoma de muchos organismos a partir de una sola muestra y los compara con bases de datos de genes conocidos. Si en el análisis aparece un gen que sabemos que pertenece a un Aspergillus, deducimos que está allí.
Este análisis también permite entender el microbioma con una lógica ecológica y evolutiva: al estudiar comunidades enteras podemos determinar qué microorganismos suelen vivir juntos, cuáles predominan cuando la piel está enferma y qué tiene que ver esto con el resto del cuerpo.
La trama se espesa
¿Por qué sufrimos diferentes enfermedades en distintas zonas de la piel? La microbiota tiene mucho que ver. Por ejemplo, la dermatitis atópica (que causa hinchazón y comezón) suele salir en el interior del codo, mientras que la psoriasis (un sarpullido con manchas rojas en la piel) afecta la parte exterior. ¿Y el acné?
Ah, el acné, ese azote de los adolescentes y muchos adultos. Aún no entendemos por completo sus causas, pero tiene que ver con la microbiota de la piel. Sabemos que es una enfermedad inflamatoria crónica, es decir que activa sin parar las células del sistema inmunitario de la piel. Se manifiesta con puntos blancos, puntos negros y áreas rojas e inflamadas cuando se obstruyen los poros. Pueden desencadenarlo cambios hormonales como los de la pubertad, el estrés o, en mujeres, los periodos menstruales, el embarazo y el uso de ciertos anticonceptivos. También pueden causarlo productos cosméticos o capilares grasosos, medicamentos como los esteroides y la testosterona, la sudoración intensa y la humedad. Tocar o frotar excesivamente la piel puede agravar el problema.
Está claro, pues, que el acné es una enfermedad multicausal con un montón de variables: genes, contaminación, hábitos… Pero cada vez se acepta más la hipótesis de que la interacción entre los microbios de la piel y la respuesta inmunitaria del cuerpo desempeña un papel crucial. Para saber más conversé con la doctora Honey Meneses, que trabaja en el Centro Dermatológico de Sinaloa y se especializa en dermatología clínica.
Honey me contó que la bacteria Cutibacterium acnes se encuentra en áreas de la piel ricas en sebo, así que durante mucho tiempo se pensó que su exceso causaba acné. Sorprendentemente, se ha descubierto que las personas con acné no tienen más bacterias C. acnes en sus folículos que las demás, pero sí están colonizadas por un tipo específico de esta bacteria, el 1A1.
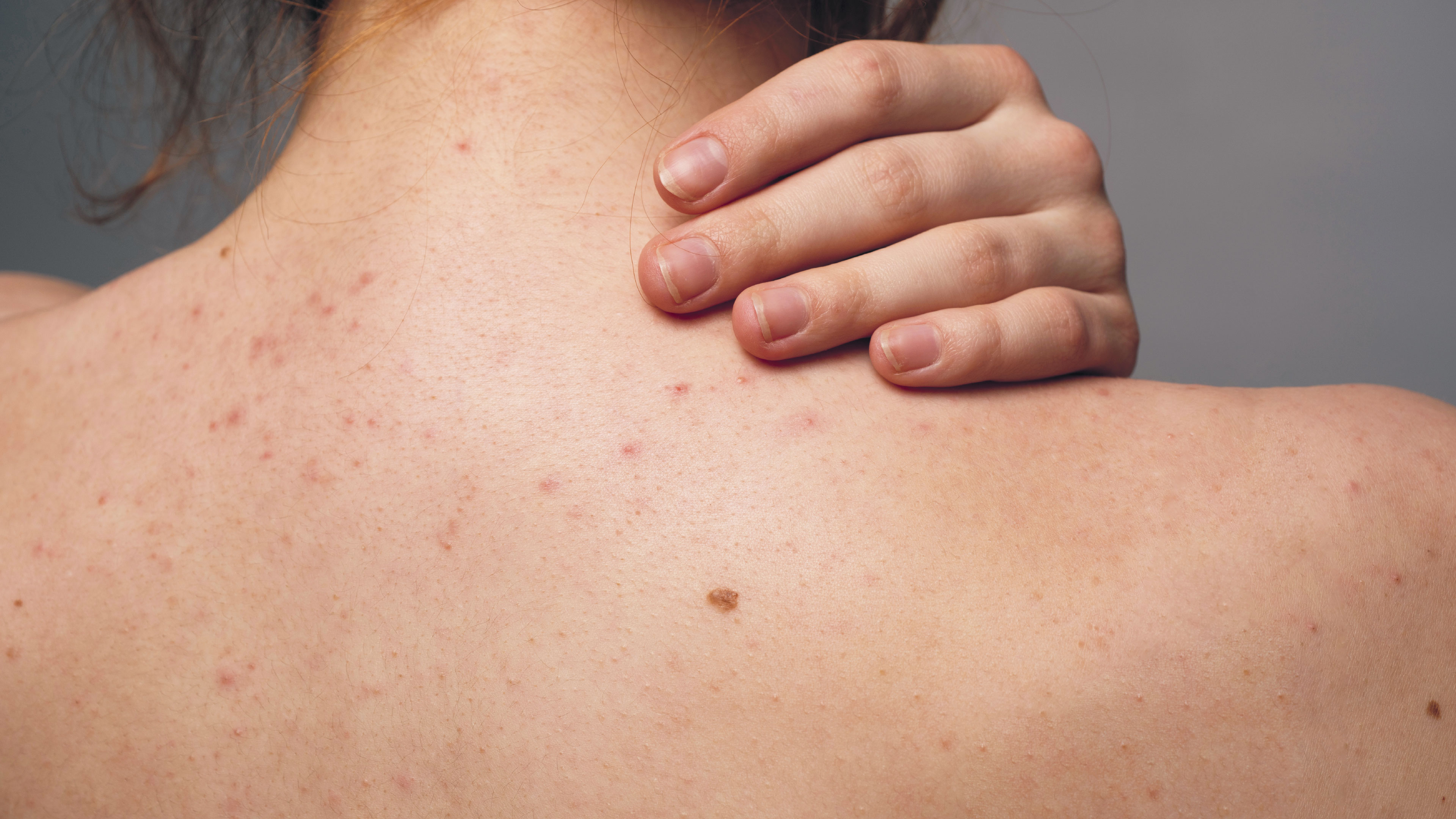 Ilustración: revista ¿Cómo ves?
Ilustración: revista ¿Cómo ves?
En condiciones saludables C. acnes protege nuestra piel de otros patógenos y ayuda a mantener el equilibrio de la microbiota cutánea. Pero se cree que una disminución en la diversidad microbiana de la piel causada por el estilo de vida y los hábitos de higiene, junto con una activación del sistema inmunitario innato (que es con el que nacemos y constituye nuestra primera línea de defensa contra patógenos invasores), podría ser lo que desencadena esta inflamación crónica. Entonces, comensales de la piel (como Lactobacillus, Burkholderia y C. acnes) se pierden y son reemplazados por géneros como Staphylococcus, Corynebacterium, otras Cutibacterium y Micrococcus. (Por cierto, hay indicios de que el microbioma de quienes viven en áreas rurales es más variable y diverso que el de los residentes urbanos.)
Afortunadamente existe un sistema de control, un organismo que equilibra la cosa cuando estamos sanos: Staphylococcus epidermidis. Esta bacteria vive en la piel y las mucosas, especialmente en lugares húmedos como axilas, ingles, narinas y conjuntivas.
S. epidermidis se ha asociado con la inhibición del crecimiento de microorganismos patógenos como Staphylococcus aureus y también puede reducir la inflamación que causa Cutibacterium acnes cuando se sale de control. Una razón más para no usar antibióticos de manera indiscriminada: pueden afectar el equilibrio natural de la microbiota de la piel y causar más problemas si barren con todo lo que hay ahí, amigo y enemigo. Imagina tomar antibióticos por un resfriado, que no te sirvan para nada y que encima te salga acné.
Honey explica que además de las microguerras que suceden en nuestra piel diariamente hay muchos otros factores que influyen en la gravedad y persistencia del acné, como el ambiente (temperatura, contaminación, humedad y luz solar), las hormonas y los antecedentes familiares. Incluso influye, sí, algo que se debatió en la comunidad científica durante años: nuestra dieta. Honey explica que se ha demostrado que las dietas altas en lácteos y alimentos con un alto índice glucémico (los que elevan rápidamente el nivel de glucosa en la sangre después de comerlos) pueden afectar la aparición y gravedad del acné.
La leche y sus derivados pueden tener proteínas como la caseína y la proteína del suero, que aumentan los niveles de una hormona llamada igf-1 y de insulina. La igf-1 puede activar procesos que aumentan la cantidad de grasa de la piel, lo que a su vez tapa los poros. Hay estudios que muestran que las personas con acné tienen niveles más altos de igf-1 que otras.
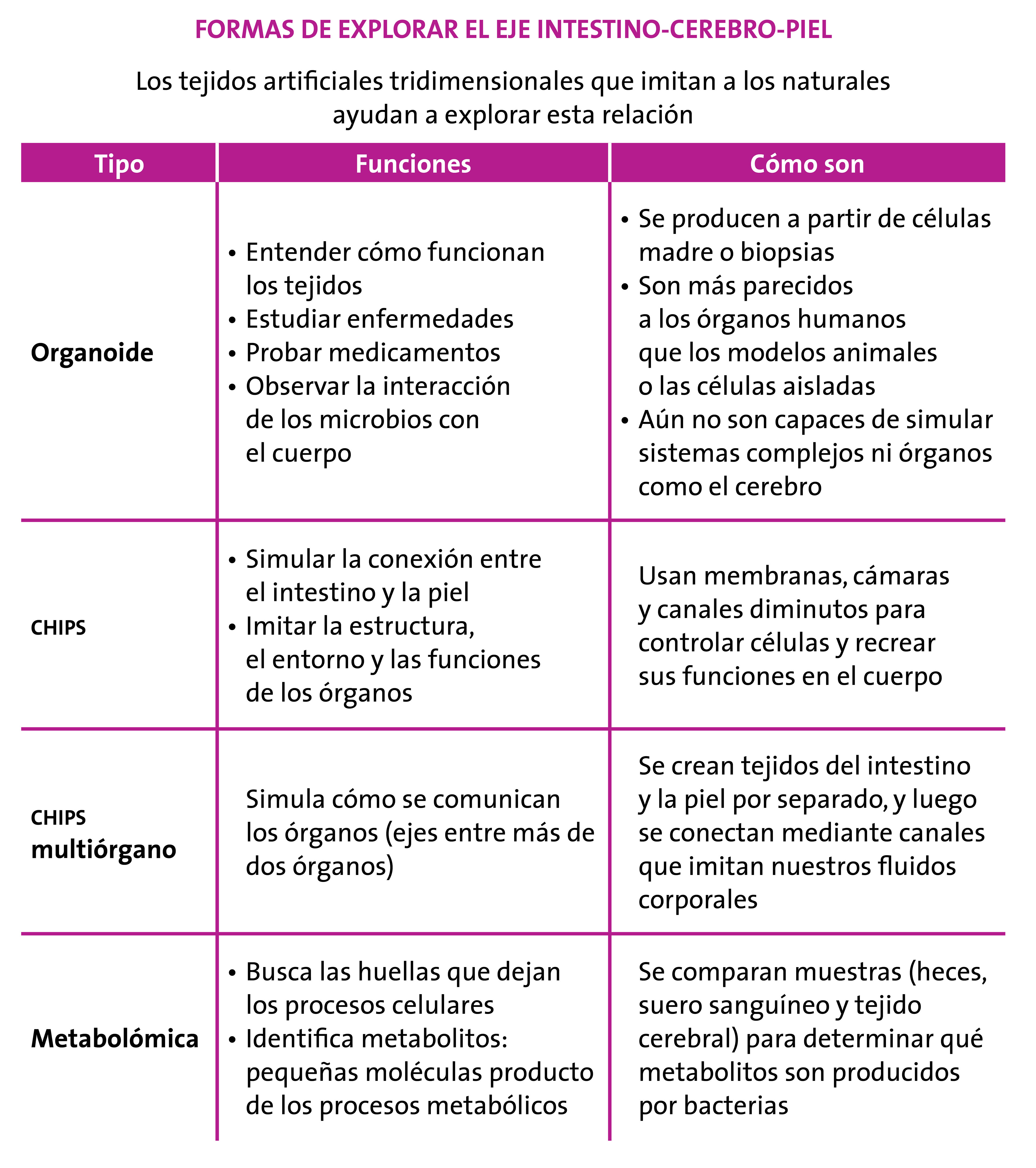
Intestino feliz, piel feliz
Si la dieta influye en el acné queda claro que el intestino y la piel se comunican de algún modo. Últimamente se habla mucho sobre el eje intestino-cerebro-piel, un mecanismo que puede trasladar el estrés psicológico del cerebro al intestino y la piel, y viceversa. Al estar en contacto directo con el entorno, nuestra piel es especialmente sensible a factores como la luz solar, la temperatura y la contaminación. En respuesta puede enviar señales al cerebro en forma de hormonas del estrés. Así, lo que afecta al cerebro también puede afectar la piel y la microbiota.
Cuando estamos estresados se activa el eje hipotálamo-hipófisis-suprarrenal (hpa, por sus siglas en inglés), un trío de glándulas que desempeñan papeles clave en la respuesta del cuerpo al estrés. Esto puede hacer que se liberen hormonas como el cortisol y las catecolaminas, que pueden atraer células inmunitarias hacia la piel y provocar reacciones como picazón o enrojecimiento. Los mastocitos, un tipo de célula de la piel, tienen un papel importante en este proceso, ya que reaccionan al cortisol.
Esto empeora el acné. Estudios en animales y humanos han demostrado que el estrés altera la microbiota intestinal, especialmente las poblaciones de bacterias como Lactobacillus y Bifidobacterium. Y aquí viene la disbiosis, cuando comensales como C. acnes se salen de control.
Mientras más vías de comunicación encontramos entre sistemas, más fácil resulta entender por qué los factores estresantes incitan a los microbios intestinales a producir sustancias cuyos efectos se trasladan a nuestros cuerpos. Desde hace tiempo sabemos que el microbioma intestinal produce neurotransmisores como acetilcolina, serotonina y norepinefrina, que atraviesan la mucosa intestinal, entran al torrente sanguíneo y causan inflamación sistémica, es decir una activación del sistema inmunitario de todo el cuerpo. (También pueden provocar cambios en el humor y se está investigando su papel en las enfermedades mentales.)
Y donde hay inflamación posiblemente habrá acné. De hecho, varios investigadores sugieren que la inflamación tiene un papel importante en todas las etapas del desarrollo de la lesión, antes de que veamos siquiera un granito.
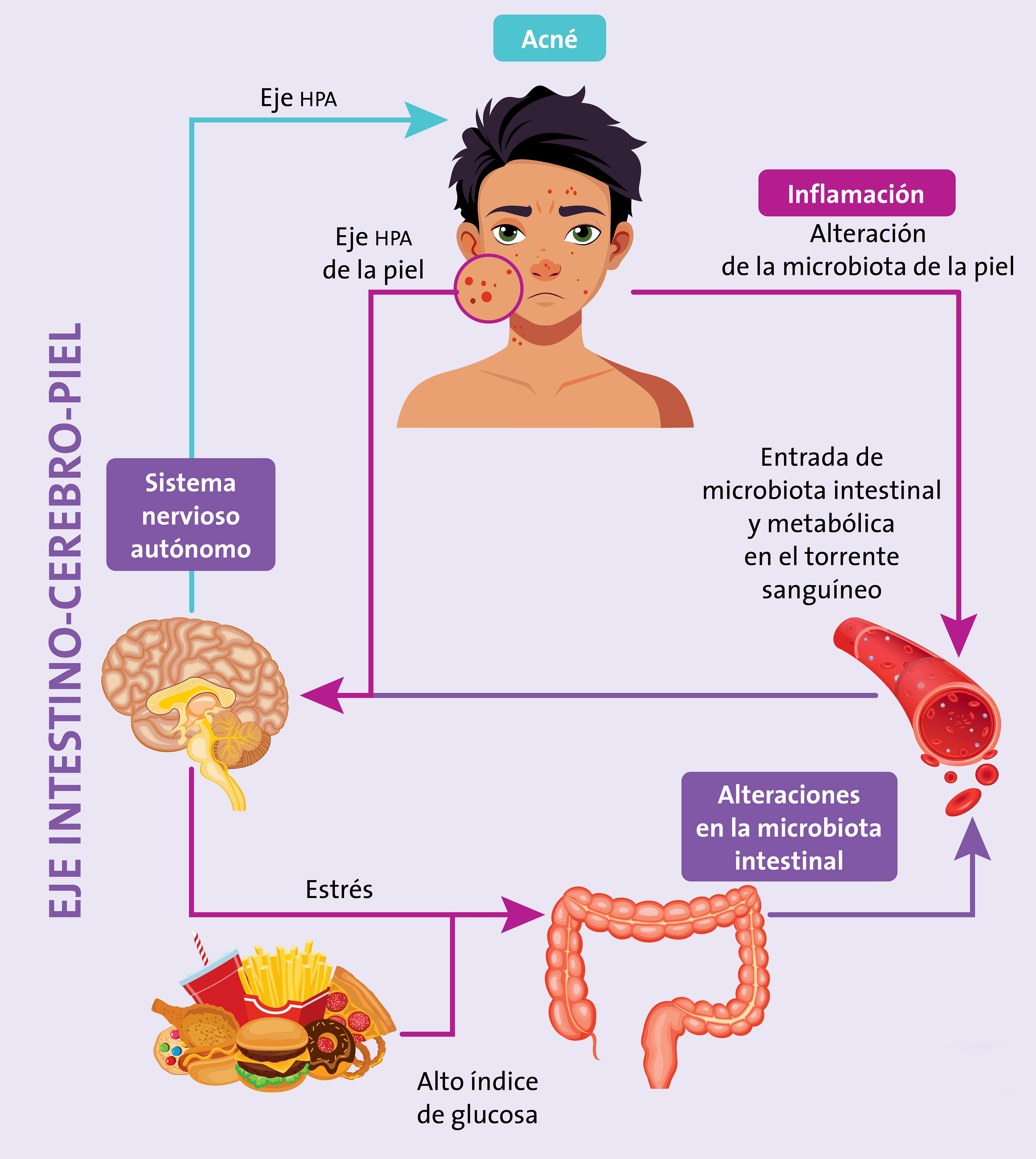
Todo esto para qué
Aunque algunos dermatólogos son escépticos debido a la falta de investigación, varios estudios han arrojado indicios de que ciertos microorganismos llamados probióticos pueden ser útiles para devolver el equilibrio entre los diferentes microbios de la piel y aliviar el acné, tanto ingeridos como aplicados sobre la piel. Hoy se sabe que probióticos como los lactobacilos y la especie Bifidobacterium bifidum pueden regular la microbiota cutánea. Incluso se habla de una posible vacuna contra el Cutibacterium acnes. Esta bacteria produce una proteína llamada hialuronidasa, que tiene dos tipos: Hyl-A, presente cuando hay acné, y Hyl-B, que está en la piel sana y ayuda a controlar los granos. La vacuna sólo atacaría a las bacterias que producen Hyl-A y dejaría intactas a las que producen Hyl-B, lo que le daría un doble efecto protector. Ya se hicieron algunas pruebas, y el acné de las personas vacunadas se redujo a la mitad en comparación con las no vacunadas.
Intervenciones como las vacunas son particularmente importantes porque sabemos que muchos tratamientos convencionales contra el acné, sobre todo los basados en antibióticos, pueden afectar las microbiotas intestinal y cutánea, provocar efectos secundarios desagradables, como descamación e irritación, y encima agravar la disbiosis. Opciones más amables son las cremas con probióticos, que ayudan a calmar estos síntomas y mantener el equilibrio de la piel.
A medida que sepamos más y tengamos datos más sólidos sobre su seguridad y eficacia podrían recomendarse terapias probióticas individualizadas. Por lo pronto, si tu piel hace cosas raras ve al dermatólogo, cuida lo que comes (puedes hacer experimentos para determinar qué alimentos exacerban el acné) y trata de controlar el estrés. El acné puede estar determinado por un desconcertante laberinto entre genes, dieta, estrés, entorno y otros factores, pero si cuidas las microvidas que nos ayudan a vivir aquí en la Tierra ¡ya harás mucho!
 Foto: Shutterstock
Foto: Shutterstock
- Andrés Cota Hiriart y Claudio H. Martínez, “Microbiota”, Masaje cerebral, 8 de junio de 2021, en: https://open.spotify.com/episode/24zPbs2fahBCzwAzcLfEUx?si=a62690e7af72481c.
- James Hamblin, Si nuestra piel hablara.La nueva ciencia de la piel, México,Grijalbo, 2022.

Mariana Mastache-Maldonado es bióloga y periodista científica. Investiga sobre neurociencias, ambiente, biomedicina y epigenética. Es ganadora del Premio Nacional de Periodismo en Salud 2024 y primer lugar en ensayo del concurso Leamos la Ciencia para Todos, del Fondo de Cultura Económica. Entusiasta de las ciudades sostenibles, el arte y la literatura.















